Ciencia
La FDA aprobó un fármaco que demostró desacelerar el deterioro cognitivo en la primera etapa del Alzheimer
La ciencia le da pelea constante al Alzheimer, una enfermedad compleja que afecta a millones de personas en todo el mundo.
La esperanza de vida sigue aumentando, como también se incrementa la cantidad de personas que viven con Alzheimer, la forma más común de demencia en personas mayores de 65 años.
A nivel global, más de 55 millones de personas (el 8,1% de las mujeres y el 5,4% de los hombres mayores de 65 años) viven con enfermedades mentales, según datos de la Organización Mundial de la Salud (OMS).
Además, se estima que esta cifra aumentará a 78 millones para 2030 y a 139 millones para 2050.
La enfermedad de Alzheimer es un trastorno neurológico que provoca la atrofia cerebral, genera la muerte progresiva de las neuronas, lo que promueve el deterioro continuo en el pensamiento, el comportamiento y las habilidades sociales que afecta la capacidad de una persona para vivir de forma independiente.
Ahora, la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó el lecanemab, un fármaco contra el Alzheimer para pacientes en las primeras fases de la enfermedad.
El fármaco pertenece a una clase de tratamientos que pretenden desacelerar el avance de la enfermedad neurodegenerativa eliminando del cerebro los grumos pegajosos de la proteína tóxica beta amiloide.
Casi todos los fármacos experimentales anteriores que usaban el mismo enfoque habían fracasado. Este fármaco está destinado a pacientes con deterioro cognitivo leve o demencia precoz de Alzheimer, una población que, según los médicos, representa un pequeño grupo de los aproximadamente 6 millones de estadounidenses que padecen actualmente la enfermedad que destruye la memoria.
El medicamento, llamado lecanemab, fue aprobado en el marco del proceso de revisión acelerada de la FDA, que apura su acceso en función de su impacto en los biomarcadores relacionados con la enfermedad subyacente que se cree que predicen un beneficio clínico.
Los expertos en Alzheimer dijeron que el fármaco ofrece beneficios modestos para los pacientes con deterioro cognitivo leve o Alzheimer en etapa temprana. Y que también conlleva algunos riesgos de hinchazón y sangrado en el cerebro que requerirán monitoreo.
Sin embargo, la enfermedad de Alzheimer no ha visto un progreso como este en décadas, por lo que, incluso -indicaron- con limitaciones, la droga es innovadora y una razón para un optimismo cauteloso.
“He hecho este diagnóstico miles de veces. He tomado muchas manos y he pasado muchos Kleenex”, dijo Jo Cleveland, médica y profesora especializada en medicina geriátrica en Wake Forest Baptist Health. La nueva aprobación “se siente como el comienzo de algo importante, como si ahora pudiéramos tomar impulso”.
Aunque no es una cura para el Alzheimer, el gran ensayo clínico publicado en noviembre mostró que el tratamiento ralentiza el deterioro cognitivo y funcional de los pacientes con Alzheimer en etapa temprana en un 27 % en comparación con el placebo.
En el estudio de 18 meses, el fármaco también redujo drásticamente los niveles de beta-amiloide, una proteína tóxica en el cerebro que se cree que impulsa el avance de la enfermedad de Alzheimer.

“La enfermedad de Alzheimer incapacita inmensamente la vida de quienes la padecen y tiene efectos devastadores en sus seres queridos”, dijo Billy Dunn, director de la Oficina de Neurociencia del Centro de Evaluación e Investigación de Medicamentos de la FDA. “Esta opción de tratamiento es la última terapia para atacar y afectar el proceso subyacente de la enfermedad de Alzheimer, en lugar de solo tratar los síntomas de la enfermedad”.
Biogen, la empresa de biotecnología con sede en Cambridge, Massachusetts, comercializará conjuntamente el fármaco con la farmacéutica japonesa Eisai, quien restringió el estudio a personas con deterioro cognitivo leve o Alzheimer en etapa temprana que también tienen evidencia de acumulación de amiloide en el cerebro, confirmada por una exploración de imágenes.
Ciencia
Científicos chinos desarrollan «Jiuzhang 4.0» y establecen nuevo récord mundial en computación cuántica

Científicos chinos desarrollaron un prototipo de computación cuántica programable llamado «Jiuzhang 4.0» que estableció un nuevo récord mundial para la tecnología de información cuántica óptica, de acuerdo con un estudio publicado hoy miércoles en la revista Nature.
Liderado por la Universidad de Ciencia y Tecnología de China (USTC), el equipo utilizó el prototipo para resolver el problema de muestreo de bosones gaussianos a una velocidad de más de 10 elevado a la 54 que la de la supercomputadora más poderosa del mundo, señala el estudio.
Los investigadores dijeron que manipularon y detectaron estados cuánticos de hasta 3.050 fotones, un salto significativo respecto a los 255 fotones alcanzados con el anterior «Jiuzhang 3.0».
Ciencia
Tratamientos avanzados para contrarrestar el párkinson
Más allá de la farmacología existen algunos tratamientos avanzados que mejoran los síntomas del párkinson. De acuerdo con el neurocirujano y especialista en radiocirugía Eduardo Lovo, este tipo de tratamientos ayuda a controlar los movimientos de las personas que lo padecen.
«Es como la versión 2.0 de los tratamientos avanzados del párkinson. Van más allá de la medicina. A muchos de los pacientes la medicina viene y les da efectos colaterales. Dentro de los más frecuentes hay movimientos anormales que los pacientes hacen, se llaman disquinesias, pero ello viene producto del tratamiento farmacológico que ingieren», acotó.
Cuando esa fase llega en los pacientes, algunos, dependiendo de las características, son candidatos para terapias avanzadas.
En el mundo de la neurocirugía, la más clásica es la técnica de estimulación cerebral profunda (DBS, por sus siglas en inglés).
«Básicamente lo que hace es que se te colocan unos electrodos en un sitio profundo del cerebro y esos electrodos se te conectan con un marcapasos cerebral. Ese estímulo eléctrico que genera el marcapasos cerebral hace que tú, por ejemplo, dejes de temblar una buena parte del día, o que la rigidez que estos pacientes desarrollan se elimine a través de un estímulo eléctrico conectado al marcapasos», explica Lovo.
Esta técnica la realizan en el sector privado, como también en el Instituto Salvadoreño del Seguro Social (ISSS), siendo pioneros en la región.
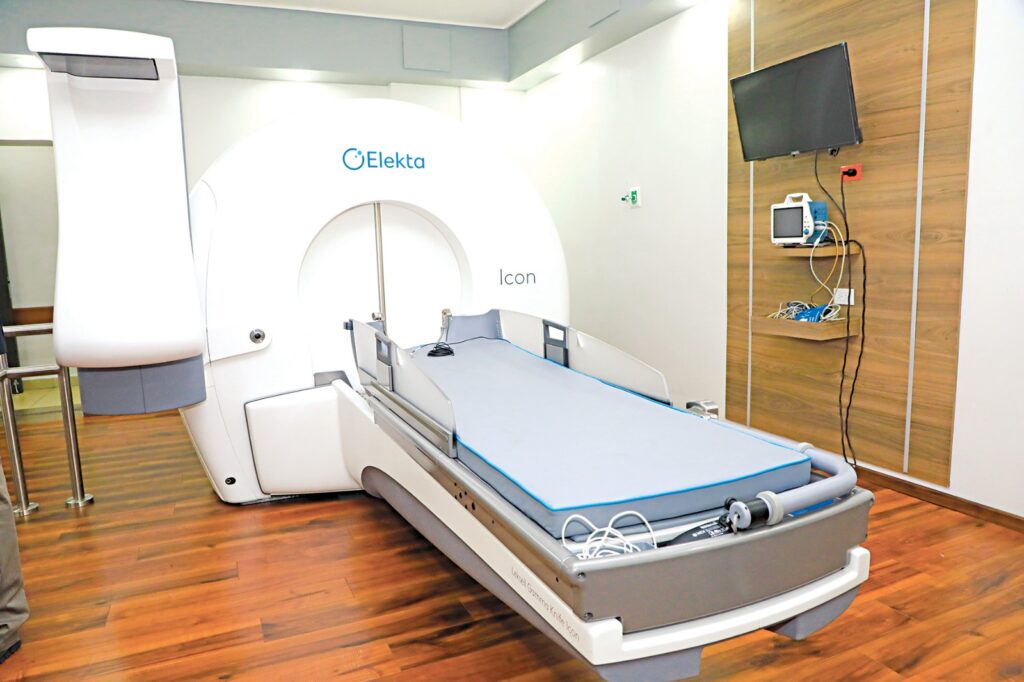
Otro que se aplica es el Gamma Knife, un procedimiento de radiocirugía estereotáctica no invasivo, seguro y ambulatorio, utilizado para tratar temblores graves y el parkinsonismo avanzado.
Mediante haces de radiación gamma focalizados, crea una lesión terapéutica precisa en el cerebro (tálamo o globo pálido) para reducir síntomas motores como el temblor. Esta técnica se aplica en El Salvador solo en el Centro Internacional del Cáncer (CIC).
El tercer tratamiento es el HIFU, que es un ultrasonido focalizado de alta intensidad para párkinson. Es un procedimiento ambulatorio no invasivo guiado por resonancia magnética que utiliza ondas sonoras para crear una pequeña lesión terapéutica en el cerebro reduciendo temblores y rigidez de forma inmediata.
Ciencia
Uso de IA permitirá detectar cáncer de páncreas hasta tres años antes del diagnóstico
Un estudio realizado por la Clínica Mayo, reconocida dentro de la comunidad médica por su atención de máxima calidad e investigaciones de vanguardia, desarrolló un modelo de inteligencia artificial (IA) que, a través de análisis de datos, flujos de trabajo en práctica, tomografías computarizadas, sistemas de imágenes y protocolos, permite asistir a especialistas para detectar cáncer de páncreas hasta tres años antes del diagnóstico clínico.
Este modelo de inteligencia artificial permite identificar signos sutiles de la enfermedad con anticipación, en la etapa donde es factible realizar un tratamiento curativo para el paciente.
El estudio fue realizado con cerca de 2,000 tomografías computarizadas a través de la asistencia de IA, que incluía a pacientes a quienes posteriormente se les diagnosticó cáncer de páncreas, que inicialmente fueron catalogados como casos «normales».
Este sistema llamado Modelo de Detección Temprana Basado en Radiómica (REDMOD) fue capaz de detectar el 73 % de los casos prediagnósticos con un promedio de 16 meses de anticipación, que figura como el doble de la tasa de detección de los especialistas que revisaron las mismas tomografías sin ayuda de la IA.
Este modelo de IA permitió detectar casi tres veces más cánceres en fase temprana que, sin la ayuda de este sistema, habrían pasado desapercibidos. REDMOD analiza cientos de características de imagen cuantitativas que detallan la textura y la estructura del tejido, identificando así cambios biológicos sutiles a medida que el cáncer comienza a desarrollarse.
Por otro lado, REDMOD está diseñado para analizar tomografías computarizadas ya realizadas por otros motivos, especialmente en pacientes de alto riesgo, como aquellos con diabetes de reciente aparición, e identificar un riesgo elevado antes de que aparezca cualquier masa visible.
Este estudio pertenece a la iniciativa Precure de la Clínica Mayo, un programa que busca redecir y prevenir enfermedades mediante la identificación de los primeros cambios biológicos en el organismo antes de que aparezcan los síntomas.












